
Año 14 Número 391
Biomarcadores en plasma para enfermedad de Alzheimer
Por Bioq. Esp. Natalia Raimondo (MP 5416)
Responsable Departamento de Inmunología – LACE Laboratorios
La enfermedad de Alzheimer (EA) es un trastorno neurodegenerativo debilitante y progresivo, y es la causa más común de demencia. Las características neuropatológicas de la EA se derivan de un procesamiento aberrante de proteínas, que conduce a la concentración de cúmulos de proteínas intraneuronales (Ovillos neurofibrilares), compuestos por filamentos helicoidales pareados de proteína tau hiperfosforilada (pTau), y agregados de proteínas extracelulares (Placas seniles); principalmente en la corteza y el hipocampo. Estos cambios neuropatológicos se asocian con pérdida sináptica y neuronal, deficiencias de neurotransmisores, neuroinflamación y astrogliosis reactiva, lo que finalmente origina un deterioro cognitivo.
El tiempo promedio entre el inicio de los síntomas y el diagnóstico de la EA es de aproximadamente 3 años; no obstante, el paciente puede haber progresado a etapas más avanzadas de la enfermedad al momento del diagnóstico. Existe un espectro de gravedad sobre la disminución de la función cognitiva en pacientes con EA, que define diferentes fases en el curso de la patología, incluyendo la enfermedad preclínica (Presencia de biomarcadores y ausencia o sutil deterioro cognitivo); la EA prodrómica (Deterioro cognitivo leve); la demencia leve y la demencia moderada a grave. El diagnóstico temprano es esencial para optimizar los beneficios de los nuevos medicamentos modificables de la enfermedad, que han demostrado aliviar sus síntomas y retrasar el deterioro clínico.
Según las recomendaciones internacionales, el diagnóstico en el ámbito clínico se limita a sujetos con fenotipos específicos de EA y hallazgos de biomarcadores que lo respalden. Las directrices establecen que pacientes con biomarcadores positivos y sin deterioro cognitivo pueden estar en un estadío preclínico. Los biomarcadores se clasifican en fisiopatológicos y topográficos; ambos pueden ayudar a profesionales médicos a reconocer, diferenciar y diagnosticar los fenotipos de la EA.
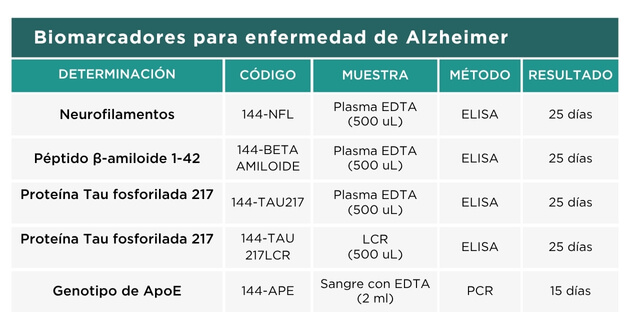
Biomarcadores fisiopatológicos: Tomografía por emisión de positrones (TEP) de amiloide, las concentraciones de proteínas amiloide y tau en el líquido cefalorraquídeo (LCR) y las concentraciones plasmáticas péptido β-amiloide (Aβ), pTau y otros biomarcadores proteicos.
Biomarcadores topográficos: Están relacionados con las consecuencias regionales de la patología de la EA, como el hipometabolismo regional en la TEP con fluorodesoxiglucosa (FDG), la TEP de tau y la atrofia regional/local en la resonancia magnética estructural (RM).
Los estudios por imágenes sólo se realizan en los grandes centros del país, es por ello que la aparición de los biomarcadores en plasma son soportes útiles en la identificación de la patología asociada a la EA; las concentraciones de péptido Aβ y pTAU en sangre han demostrado asociaciones con las correspondientes en LCR y con la positividad en PET. Recientemente, se han desarrollado varios ensayos de alta sensibilidad que permiten detectar de manera fidedigna diferentes isoformas de p-tau en plasma, incluidas p-tau181, p-tau217 y p-tau231. La proteína p-tau217 mostró un mejor rendimiento, con alta correlación entre los niveles plasmáticos y de LCR.
El péptido Aβ es un producto de la escisión proteolítica de la proteína precursora amiloide (APP) por la acción secuencial de las β- y γ-secretasas. Dependiendo del sitio de escisión, se producen distintas isoformas de Aβ. La forma principal de Aβ contiene 40 aminoácidos (Aβ1-40). La isoforma de 42 residuos (Aβ1-42) es menos frecuente que Aβ1-40, pero se agrega más rápidamente y se deposita mucho antes en el proceso de la enfermedad, respecto a Aβ1-40, constituyendo el componente principal de las placas seniles. Las concentraciones elevadas de Aβ1-42 en plasma están asociadas con la presencia de demencia tipo EA, riesgo de progresión de deterioro cognitivo y depósitos de péptidos Aβ cerebrales o atrofia cortical estructural en las RM.
Varios autores demostraron que altos niveles de neurofilamentos plasmáticos son indicadores de neurodegeneración activa en algunos trastornos neurodegenerativos, entre ellos la EA. Además, la apolipoproteína E (APOE) es un biomarcador genético sanguíneo, y el genotipo APOE ε4 representa un factor de riesgo para la EA. Una de las condiciones que puede elevar la progresión a EA sintomática es el estado de portador del gen APOE ε4, siendo los homocigotos APOE ε4 un riesgo muy alto para desarrollar EA clínica. Por lo tanto, la presencia de APOE ε4 en un individuo con síntomas compatibles con EA respalda la probable aparición de patología amiloide.
Los biomarcadores son indicadores clave de triaje en la detección de la EA, que permiten identificar tempranamente a los pacientes que requieren una evaluación neurocognitiva y pruebas confirmatorias.
La incorporación de estos marcadores plasmáticos en LACE Laboratorios potencia la práctica clínica, aportando información que orienta decisiones diagnósticas más precisas y un abordaje ajustado a cada persona.
Referencias:
Zecca C, Tortelli R, Panza F, et al. Plasma β-amyloid1-42 reference values in cognitively normal subjects. J Neurol Sci. 2018 Aug 15;391:120-126. doi: 10.1016/j.jns.2018.06.006. Epub 2018 Jun 13. PMID: 30103961.
Dubois B, von Arnim CAF, Burnie N, et al. Biomarkers in Alzheimer’s disease: role in early and differential diagnosis and recognition of atypical variants. Alzheimers Res Ther. 2023 Oct 13;15(1):175. doi: 10.1186/s13195-023-01314-6. PMID: 37833762; PMCID: PMC10571241.
Hansson O, Blennow K, Zetterberg H, et al. Blood biomarkers for Alzheimer’s disease in clinical practice and trials. Nat Aging. 2023 May;3(5):506-519. doi: 10.1038/s43587-023-00403-3. Epub 2023 May 18. PMID: 37202517; PMCID: PMC10979350.
Lombardi G, Pancani S, Manca R, et al. Role of Blood P-Tau Isoforms (181, 217, 231) in Predicting Conversion from MCI to Dementia Due to Alzheimer’s Disease: A Review and Meta-Analysis. Int J Mol Sci. 2024 Nov 30;25(23):12916. doi: 10.3390/ijms252312916. PMID: 39684623; PMCID: PMC11641364.
Frisoni GB, Hansson O, Nichols E, et al. New landscape of the diagnosis of Alzheimer’s disease. Lancet. 2025 Sep 27;406(10510):1389-1407. doi: 10.1016/S0140-6736(25)01294-2. Epub 2025 Sep 22. PMID: 40997838.
Fox NC, Belder C, Ballard C, et al.Treatment for Alzheimer’s disease. Lancet. 2025 Sep 27;406(10510):1408-1423. doi: 10.1016/S0140-6736(25)01329-7. Epub 2025 Sep 22. PMID: 40997839.

LACE CENTRAL:
Av. Vélez Sarsfield 528 - Córdoba
DERIVACIONES CLÍNICAS:
Teléfono: 0810 222 5223
Celular: + 54 9 351 7357947
WhatsApp: + 54 9 351 3209988
derivaciones@laboratoriolace.com.ar
DERIVACIONES LACEVET
Teléfono: 0810 222 5223
Celular +54 9 351 3528462
WhatsApp + 54 9 351 3209988
derivaciones@laboratoriolace.com.ar
LACE JARDÍN: Bv. Elías Yofre 1286
LACE CERRO: Av. Rafael Núñez 4436
LACE MAIPÚ: Av. Amadeo Sabattini 2143
LACE GENERAL PAZ: Gral. M. Güemes 207
LACE RUTA 20: Av. Fuerza Aérea 2751
LACE VILLA ALLENDE:Enrique Bodereau 9852
LACE RÍO CUARTO: Pedernera 459
LACE CARLOS PAZ: Av. Sabattini 77
